Avastin
Avastin: brugsanvisning og anmeldelser
- 1. Frigør form og sammensætning
- 2. Farmakologiske egenskaber
- 3. Indikationer for brug
- 4. Kontraindikationer
- 5. Påføringsmetode og dosering
- 6. Bivirkninger
- 7. Overdosering
- 8. Særlige instruktioner
- 9. Påføring under graviditet og amning
- 10. Brug til ældre
- 11. Lægemiddelinteraktioner
- 12. Analoger
- 13. Vilkår og betingelser for opbevaring
- 14. Betingelser for udlevering fra apoteker
- 15. Anmeldelser
- 16. Pris på apoteker
Latinsk navn: Avastin
ATX-kode: L01XC07
Aktiv ingrediens: Bevacizumab (Bevacizumab)
Producent: F. Hoffmann-La Roche Ltd. (Schweiz), Roche Diagnostics (Tyskland), Genentech Inc. (USA)
Beskrivelse og fotoopdatering: 16-09-2019
Priser på apoteker: fra 8755 rubler.
Købe
Avastin er et antineoplastisk middel og tilhører monoklonale antistoffer. Brug af lægemidlet hjælper med at undertrykke den metastatiske progression af sygdommen og reducere mikrovaskulær permeabilitet i forskellige typer tumorer (bryst, prostata, bugspytkirtel, tyktarmskræft).
Frigør form og sammensætning
Avastin fås i form af et koncentrat beregnet til fremstilling af en opløsning til infusion, det kan have en lysebrun farve eller være farveløs.
Den aktive ingrediens i lægemidlet er bevacizumab.
Denne medicin fås i pakninger, der indeholder 100 mg / 4 ml og 400 mg / 16 ml bevazumab.
Farmakologiske egenskaber
Farmakodynamik
Avastin er et humaniseret rekombinant hyperchimært monoklonalt antistof, der selektivt binder til og neutraliserer vaskulær endotelvækstfaktor (VEGF), som har biologisk aktivitet. Bevacizumab, den aktive komponent i lægemidlet, hæmmer bindingen af vaskulær endotelvækstfaktor til dets receptorer af type 1 og 2 (Flt-1, KDR) placeret på overfladen af endotelceller. Dette fører til et fald i vaskularisering og undertrykkelse af tumorvækst.
Bevacizumab indeholder fuldt humane rammeregioner med komplementaritetsbestemmende regioner af mushyperkimært antistof, der binder til VEGF. Denne forbindelse produceres ved hjælp af rekombinant DNA-teknologi i et kinesisk hamster-ovariecelleekspressionssystem. Bevacizumab har en længde på 214 aminosyrer og har en molekylvægt på ca. 149.000 dalton.
Introduktionen af Avastin tilvejebringer hæmning af metastatisk progression af sygdommen og reducerer mikrovaskulær permeabilitet i forskellige humane kræftformer, herunder kræft i prostatakirtlen, bugspytkirtlen, brystet og tyktarmen.
Bevacizumabs kræftfremkaldende og mutagene potentiale forstås ikke godt. Da det blev administreret til dyr, blev der registreret embryotoksiske og teratogene virkninger på kroppen. Anvendelsen af lægemidlet hos dyr, der gik ind i det aktive vækststadium og har åbne vækstzoner, blev ofte ledsaget af dysplasi i bruskpladen.
Farmakokinetik
Farmakokinetikken for bevacizumab kan beskrives ved hjælp af en model med to kammer. Fordelingen af stoffet er kendetegnet ved en lav clearance, et lavt distributionsvolumen i det centrale kammer og en lang halveringstid, hvilket muliggør opretholdelse af den nødvendige terapeutiske plasmakoncentration af Avastin under infusionen en gang hver 2-3 uger.
Clearance af bevacizumab er ikke relateret til patientens alder. Det er også 30% højere hos patienter med lave albuminniveauer og 7% højere hos patienter med signifikant tumormasse sammenlignet med patienter med gennemsnitlige albuminkoncentrationer og tumormasseværdier.
Distributionsvolumen er henholdsvis 3,28 liter og 2,73 liter hos mænd og kvinder, hvilket svarer til fordelingsvolumenet af klasse G immunoglobuliner (IgG) og andre monoklonale antistoffer. Distributionsvolumenet i det perifere kammer når 2,35 liter og 1,69 liter for henholdsvis mænd og kvinder, når Avastin kombineres med andre kræftlægemidler. Efter dosisjustering for kropsvægt hos mandlige patienter er fordelingsvolumenet 20% større end hos kvinder.
Efter en enkelt intravenøs indgivelse af 125I -bevacizumab er dets metaboliske egenskaber identiske med egenskaberne for et naturligt IgG-molekyle, der ikke binder til VEGF. Metabolismen og udskillelsen af den aktive komponent i Avastin svarer fuldt ud til metabolismen og udskillelsen af endogent IgG, det vil sige de overvejende udføres gennem proteolytisk katabolisme i alle celler i kroppen, inklusive endotelceller, og ikke gennem leveren og nyrerne. IgG binder til neonatale receptorer til det krystalliserende fragment af IgG (FcRn-receptorer), hvilket fjerner det fra processerne med cellulær metabolisme og giver en lang halveringstid.
Farmakokinetikken for bevacizumab er lineær i intervallet af doser taget 1,5-10 mg / kg pr. Uge. Clearance for denne forbindelse er 0,22 l / dag for mænd og 0,188 l / dag for kvinder. Efter dosisjustering baseret på kropsvægt øges clearance af bevacizumab hos mænd med 17% sammenlignet med kvindelige patienter. Halveringstiden for stoffet hos mænd er 20 dage, hos kvinder - 18 dage.
Farmakokinetikken for bevacizumab afhænger ikke af patientens alder. Data om stoffets farmakokinetik, når det anvendes til børn og unge, er begrænsede. De tilgængelige data viser, at der ikke er nogen forskel mellem clearance og distributionsvolumen for bevacizumab hos børn, unge og voksne patienter med signifikante tumorer. Virkningen og sikkerheden af Avastin hos patienter med lever- og / eller nyreinsufficiens har været lidt undersøgt, da nyrerne og leveren ikke er de vigtigste organer, hvori metabolismen og den efterfølgende udskillelse af bevacizumab udføres.
Indikationer til brug
I henhold til instruktionerne er Avastin ordineret til:
- Metastatisk eller lokalt tilbagevendende brystkræft;
- Avanceret, inoperabel, metastatisk eller tilbagevendende ikke-squamous celle, ikke-småcellet lungekræft;
- Avanceret og / eller metastatisk nyrecellekarcinom;
- Metastatisk kolorektal kræft;
- Tilbagevendende glioblastom.
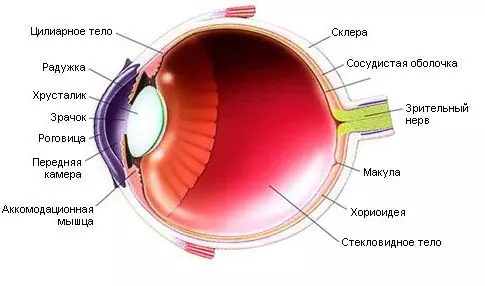
Anvendelsen af Avastin i oftalmologi skyldes dets effektivitet til behandling af den våde form for aldersrelateret makuladegeneration, makulaødem, tumorer i den perimakulære region, diabetisk retinopati og nogle andre øjensygdomme, der er relateret til den patologiske vækst i blodkar. Resultaterne af injektioner i glaslegemet beviser effektiviteten af denne procedure og dens gode tolerabilitet hos patienter med proliferativ diabetisk retinopati. Effekten af at bruge Avastin i oftalmologi er at stabilisere den subretinale neovaskulære membran. Bivirkninger fra injektionen af lægemidlet i glaslegemet er minimale.
Kontraindikationer
Avastin bør ikke anvendes til behandling af patienter med overfølsomhed over for lægemiddelkomponenterne såvel som gravide og ammende kvinder. Bevacizumab-behandling er kontraindiceret hos børn og personer med nyre- og leverinsufficiens, da lægemidlets virkning og sikkerhed i forhold til sådanne patienter ikke er fastslået. Alle ovennævnte kontraindikationer er også relevante, når du bruger dette lægemiddel i oftalmologi.
Instruktioner til brug af Avastin: metode og dosering
Intravenøs injektion af lægemidlet er strengt forbudt, det er kun tilladt at injicere Avastin intravenøst dryp. Fortynding af den krævede mængde koncentrat til det krævede volumen sker ved hjælp af 0,9% natriumchloridopløsning, mens alle sterilitetsregler tages i betragtning. Den tilberedte formulering skal indeholde bevacizumab i intervallet 1,4-16,5 mg / ml. Den indledende dosis Avastin administreres efter kemoterapi som en intravenøs infusion i 90 minutter, brug af efterfølgende doser er mulig både efter og før kemoterapi. Hvis patienten tolererede den første infusion godt, reduceres tiden til introduktion af den anden til 60 minutter, og hvis positive reaktioner vedvarer, udføres efterfølgende Avastin-infusioner inden for 30 minutter. I tilfælde af bivirkninger bør brugen af Avastin stoppes helt eller midlertidigt.
Standard dosering
Til metastatisk kolorektal kræft:
- Som et førstelinjemedicin: 5 mg pr. 1 kg kropsvægt 1 gang i 2 uger eller 7,5 mg pr. 1 kg kropsvægt 1 gang på 3 uger intravenøst, langsomt.
- Som et andet linjemedicin, 5 til 10 mg pr. Kg legemsvægt, en gang hver anden uge, intravenøst, langsomt.
Med lokalt tilbagevendende eller metastatisk brystkræft, 10 mg pr. 1 kg kropsvægt intravenøst en gang hver anden uge langsomt.
Til almindelig inoperabel, tilbagevendende eller metastatisk ikke-squamous celle lungekræft ordineres Avastin i en dosis på 7,5 til 15 mg pr. Kg kropsvægt en gang hver tredje uge, afhængigt af hvilken type kemoterapi der ordineres ud over lægemidlet.
Til avanceret og / eller metastaserende nyrecellekarcinom ordineres lægemidlet i en dosis på 10 mg pr. Kg kropsvægt en gang hver anden uge intravenøst, langsomt.
Til glioblastom (grad IV gliom) ordineres Avastin i en dosis på 10 mg pr. Kg kropsvægt en gang hver anden uge intravenøst, langsomt.
I epitelcancer i æggestokken, æggelederen såvel som i primær kræft i bughinden, ordineres lægemidlet i en dosis på 15 mg pr. Kg kropsvægt en gang hver tredje uge intravenøst, langsomt.
Som et førstelinjemedicin ordineres Avastin ud over carboplatin og paclitaxel, mens den maksimale varighed af kemoterapi er 6 cyklusser, hvorefter Avastin fortsættes som monoterapi.
Den samlede varighed af behandlingen med dette lægemiddel er 15 måneder. Hvis der vises symptomer på sygdomsprogression, bør Avastin-behandlingen ikke fortsættes.
I tilfælde af tilbagefald af tumor ordineres Avastin i kombination med carboplatin og gemcitabin (løbet af 6-10 cyklusser), derefter anvendes lægemidlet som monoterapi.
Bivirkninger
Anmeldelser af Avastin indikerer, at de mest alvorlige bivirkninger manifesteres i form af perforering af mave-tarmkanalen, blødning, herunder lungeblødning eller hæmoptyse og arteriel tromboembolisme. Du kan også ofte finde klager over forhøjet blodtryk, diarré, mavesmerter, svaghed eller asteni. Instruktionerne til Avastin, ud over de nævnte, angiver følgende mulige manifestationer af bivirkninger ved administration af medicinen:
- Forhøjet blodtryk, arteriel tromboemboli, dyb venetrombose, kongestiv hjertesvigt, blødning;
- Neutropeni, leukopeni, febril neutropeni, trombocytopeni, anæmi;
- Forstoppelse, diarré, opkastning, kvalme, rektal blødning, anoreksi, stomatitis;
- Tarmobstruktion, gastrointestinale lidelser, mavesmerter, perforering af mave-tarmkanalen;
- Rhinitis, epistaxis, åndenød, hypoxi, lungetromboembolisme;
- Tør hud, misfarvning, eksfoliativ dermatitis, palmar-plantar syndrom;
- Øget lakrimation, nedsat synsfunktion;
- Artralgi, myalgi, muskelsvaghed;
- Proteinuri, urinvejsinfektion;
- Asteni, feber, øget træthed, smerter ved forskellig lokalisering, byld, dehydrering, sepsis.
Det er også muligt at reducere niveauet af hæmoglobin, udseendet af hyperglykæmi, leukopeni, hypokalæmi, trombocytopeni.
Overdosis
Ved intravenøs administration af Avastin i en maksimal dosis på 20 mg / kg hver anden uge, bemærkes i nogle tilfælde svær hovedpine (migræne). Overdosering kan også føre til øgede bivirkninger, som er dosisafhængige. Der er ingen specifik modgift, så symptomatisk behandling udføres.
specielle instruktioner
I løbet af behandlingen med Avastin og mindst seks måneder efter det skal kvinder og mænd i den fødedygtige alder anvende pålidelige svangerskabsforebyggende midler. På trods af indholdet i instruktionerne med al den nødvendige information, skal udnævnelsen, klargøringen af opløsningen og dens dosering kun udføres af en erfaren specialiseret læge.
Farmaceutiske egenskaber ved bevacizumab er uforenelige med dextroseopløsning.
Påføring under graviditet og amning
Graviditet og amning er kontraindikationer for udnævnelsen af Avastin. Mænd og kvinder i reproduktiv alder rådes kraftigt til at bruge pålidelige præventionsmetoder under lægemiddelbehandling og i mindst 6 måneder efter afslutningen af behandlingen.
Avastin kan føre til fertilitetsproblemer hos kvinder. Hos de fleste patienter gendannes fertiliteten efter tilbagetrækning af lægemidlet. De langsigtede konsekvenser af lægemiddelbehandling med hensyn til dens virkning på fertiliteten forbliver ukendte. Under behandling med lægemidlet og i mindst 6 måneder efter dets afslutning er det nødvendigt at stoppe amningen.
Brug til ældre
Avastin ordineres med forsigtighed til ældre patienter (over 65 år).
Lægemiddelinteraktioner
Kliniske studier viser, at kombinationen af Avastin med kemoterapikurser praktisk talt ikke har nogen effekt på lægemidlets farmakokinetik. Klinisk eller statistisk signifikante forskelle i lægemiddelclearance hos patienter, der fik monoterapi, og hos patienter, hvor Avastin blev brugt i kombination med interferon alfa-2a eller andre kemoterapi-lægemidler (cisplatin / gemcitabin, FU / LV, IFL, doxorubicin, capecitabin, carboplatin / paclitaxel) blev ikke identificeret.
Brug af lægemidlet påvirker ikke de farmakokinetiske egenskaber af irinotecan og dets aktive metabolit (SN38), cisplatin, capecitabin og dets metaboliske produkter, interferon alfa-2a, oxaliplatin (bestemt af det samlede og frie platinindhold). Der er ingen pålidelige data om effekten af Avastin på gemcitabins farmakokinetik.
Når lægemidlet kombineres i en dosis på 10 mg / kg en gang hver anden uge og sunitinib (50 mg hver dag) hos patienter med nyrecellecarcinom af metastatisk type, observeres undertiden tilfælde af mikroangiopatisk hæmolytisk anæmi, manifesteret af trombocytopeni, anæmi og fragmentering af erytrocytter. I isolerede tilfælde har patienter også arteriel hypertension, herunder hypertensiv krise, øgede kreatininniveauer og neurologiske lidelser. Disse symptomer er reversible og forsvinder næsten efter seponering af sunitinib- og bevacizumab-behandlingen.
Når Avastin ordineres som et supplement til strålebehandling og kemoterapi (temozolomid) hos patienter med oprindeligt diagnosticeret glioblastom, ændres lægemidlets sikkerhedsprofil ikke.
Effekten og sikkerheden af Avastin som supplement til strålebehandling ved andre indikationer er ikke blevet fastslået. Lægemidlet er kendt for farmaceutisk uforenelighed med dextroseopløsninger.
Analoger
Analoger af Avastin, som er tæt på virkningsmekanismen, der tilhører en farmakologisk undergruppe, inkluderer: Vectibix, Herceptin, Campas, Mabthera, Erbitux, Arserra, Removab, Perieta, Herceptin lyophilisate, Rituximab, Acellbia, Mabtera.
Der er ingen analoger af lægemidlet til den aktive ingrediens.
Vilkår og betingelser for opbevaring
Avastin skal opbevares på et mørkt sted ved en temperatur på 2-8 ° C. Den færdige opløsning betragtes som egnet til brug i løbet af dagen.
Betingelser for udlevering fra apoteker
Udleveres efter recept.
Anmeldelser om Avastin
Ifølge anmeldelser virker Avastin på kroppen på forskellige måder. Mange patienter rapporterer om en signifikant forbedring i deres tilstand og et fald i tumorens størrelse, men fuldstændig bedring er næsten umulig. Patienter klager også ofte over bivirkninger af lægemidlet: stigninger i blodtryk, hovedpine og lejlighedsvis synshandicap op til fuldstændig blindhed. De tiltrækkes ikke af de høje omkostninger ved lægemidlet.
Prisen på Avastin på apoteker
Den omtrentlige pris for Avastin (1 flaske 16 ml) er i gennemsnit 22.050-24.500 rubler.
Avastin: priser på onlineapoteker
|
Lægemiddelnavn Pris Apotek |
|
Avastin 100 mg / 4 ml koncentrat til fremstilling af infusionsvæske, opløsning 4 ml 1 stk. 8755 RUB Købe |
|
Avastin 400 mg / 16 ml koncentrat til fremstilling af infusionsvæske, opløsning 16 ml 1 stk. 36.770 RUB Købe |

Maria Kulkes Medicinsk journalist Om forfatteren
Uddannelse: Det første medicinske universitet i Moskva opkaldt efter I. M. Sechenov, specialitet "General Medicine".
Oplysninger om lægemidlet er generaliseret, kun til informationsformål og erstatter ikke de officielle instruktioner. Selvmedicinering er sundhedsfarligt!